Qué es el pH
El pH es un parámetro que se utiliza para medir el grado de acidez de una sustancia. A través de este se logra determinar la concentración de hidrogeniones (ion positivo de Hidrógeno) en una disolución.
El término se encuentra formado por dos letras que las cuales significan:
- p: potencial.
- H: hidrógeno.
Escala de pH
La escala de pH es una forma precisa de clasificar la acidez, basicidad o neutralidad de una solución.
La escala del potencial de hidrogeniones fue creada por Soren Peter Lauritz Sorensen (1868-1939), un bioquímico danés nacido en Haure Bjerg.
La concentración de iones de hidrógeno (protones) jugó un papel clave en las reacciones enzimáticas, por lo que en 1909 ideó una forma simple de expresarlo, que era calcular el logaritmo negativo de dicha concentración. De esta manera, se obtuvieron valores simples y manejables dentro de una escala conveniente, que él llamó pH.
Se utiliza para determinar la naturaleza ácida o básica de la solución, para determinar la concentración de iones hidronio presente en una solución y para averiguar la neutralidad de una solución.
La secuencia que tiene la escala del pH es logarítmica, lo que quiere decir que la diferencia entre una unidad numérica y otra puede ser 10 veces más básica o ácida dependiendo del caso.
Los valores en la escala de pH son multiplicados por 10 en cada unidad. Es decir, que el valor del potencial de hidrogeniones de 6 es 10 veces más ácido que un pH con un valor de 7, pero un potencial de hidrogeniones de 5 es 100 veces más ácido que un pH de 7.
La escala de potencial de hidrogeniones está numerada desde el 1 hasta el 14, entre el 1 y el 6 significa que la sustancia es más ácida, el 7 es el caso del agua destilada y tiene un valor neutro, y del 8 al 14 significa que la sustancia es más alcalina.
Tabla de pH
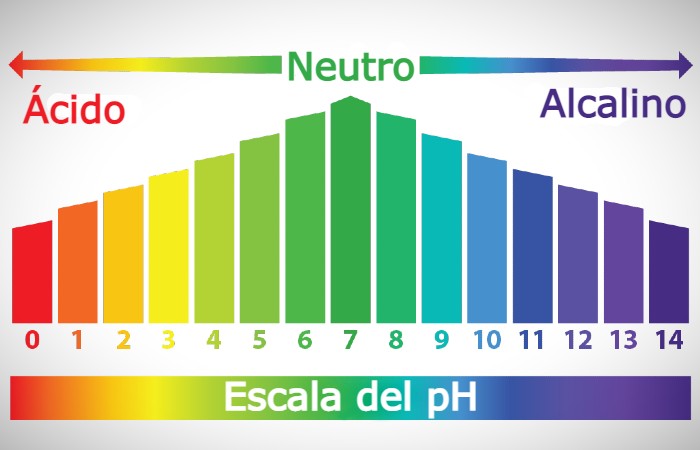
Indicadores de pH
Los indicadores de pH son los diferentes medios que se utilizan para determinar el potencial de hidrogeniones de una sustancia. Existen tres tipos que son, indicadores líquidos, papeles indicadores y pH metros.
Indicadores líquidos

Son bases orgánicas que poseen diferentes colores que varían según su forma ácida. Trabajan en rangos limitados, varían su color y dejan de variar cuando alcanza el máximo nivel de dicho rango. Debe ser usado solo en soluciones incoloras, para poder observar el cambio de color.
Estos indicadores son muy utilizados en las titulaciones química analítica, pero se debe contar con un nivel de entrenamiento para lograr que esta práctica sea precisa.
pH-metro
Estos surgen por la necesidad de los laboratorios y sus analistas, de obtener valores exactos desde este parámetro, algo que no se logra con los indicadores líquidos, ni los de papel. Está basado en la medición del diferencial de potencial eléctrico entre el pH del electrodo y el electrodo referencial.
Este equipo está conformado por dos electrodos, uno de estos es metálico e insensible al pH de la solución, más un amplificador electrónico sencillo. Su calibración se realiza con soluciones de pH conocidos, que sirven para leer sustancias.
Papeles indicadores
Se trata de un papel tornasol (este es elaborado con un polvo proveniente de líquenes) que debe entrar en contacto con la solución de una manera discreta, para poder analizar y medir su precisión.
Este papel sirve para saber si una solución líquida o gaseosa es básica o ácida, su presentación es en dos colores, rojo y azul.
Cuando se trata de una solución líquida, el papel no debe ser introducido por completo en ella, el proceso es colocar gotas o tocar el líquido de una manera muy breve.
Cuando la solución es gaseosa, se debe pasar el gas sobre la superficie de papel, para que de esta manera cambie de color.
Importancia del pH
El hombre en su día a día utiliza muchos productos químicos que podrían resultar peligrosos, es por esta razón que se debe realizar una medición de pH, para probar su grado de acidez y el riesgo que se puede correr al utilizarlos.
Al ingerir alimentos se altera el pH del cuerpo. El estómago de una persona tiene un pH de 1-4 ya que éste ácido es necesario para la descomposición de los alimentos. Algunos alimentos pueden ocasionar que el estómago genere más ácido, ésto es muy común y dicho ácido puede llegar a perforar las paredes del estómago y causar úlceras. Su exceso podría llegar hasta el esófago, llegar hasta la boca y ocasionar lo que comúnmente se conoce como acidez, por esto se debe cuidar la calidad de los alimentos que se consumen.
Es muy importante mantener un pH equilibrado ya que esto permitira el buen funcionamiento del organismo.
En el ambito empresarial, el ph es fundamental en los procesos industriales, ya que de existir una minima variacion en sus niveles, puede llegar a afectar negativamente la calidad del producto.
En la agricultura es un factor importante al momento de determinar si el suelo tiene las condiciones necesarias para la siembra.
Ejemplos de pH
Algunos de los pH más conocidos son:
- pH del agua: en el caso del agua no ionizada (pura) su valor es 7.
- pH de la sangre: su valor ideal es aquel que oscila entre 7,35 y 7,45. Sin embargo, es normal que este valor sea alterado por factores como malos hábitos alimenticios, el estrés o incluso la contaminación atmosférica.
- pH del limón: su valor se encuentra entre 2,2 y 2,4.
- pH de la leche: su valor ideal es de 6,7. Mientras más bajo sea el valor, mayor será la degradación de bacterias en la leche.
- pH de la orina: entre 4,6 y 8,0 para los valores normales.
- pH del vinagre: su valor suele encontrarse entre 2,5 y 3,0. Este valor depende de que tan concentrado sea el ácido acético presente.
- pH del bicarbonato de sodio: su valor normal es de 9, aunque todo depende de la concentración con la que sea elaborado.
- pH del estómago: este se encuentra entre 1,0 y 3,0. En el caso del intestino grueso su valor es de 8,0 y para el intestino delgado se encuentra entre 5,0 y 7,0.
- pH del suelo: su valor se encuentra en el rango entre 6,5 y 7,0.
- pH de la saliva: posee un valor comprendido entre 6,7 a 7,4.
- pH del aguacate: posee un valor de 15,6.
- pH del café: este valor sirve para determinar la calidad del café. El valor ideal se encuentra entre 4,9 y 5,2. Por encima de este rango se torna más amargo, mientras que por debajo es un café más ácido.
- pH vaginal: entre 4,5 y 5 durante el tiempo en el cual la mujer es fértil. Durante la menopausia y la menstruación sube y se encuentra entre 6,8 y 7,2.
- pH de la piel: su valor óptimo, tanto para el cuerpo como para la cara, va desde 4,7 hasta 5,75.
- pH del cloro: este se encuentra en un rango comprendido entre 7,0 y 7,7.
- pH del jabón: cuando tiene un valor de 7 se considera neutro, sin embargo, la mayoría de los que son vendidos como neutros en realidad tienen un valor de 5,5, similar al de la piel de las personas.






